El pH del agua

Todos sabemos que el pH del agua es una medida de su mayor o menor acidez o alcalinidad, que un pH de 7 es neutro, y que son ácidos los inferiores a 7 y alcalinos los superiores a esa cifra, y que el pH es de extraordinaria importancia para la salud de los peces e invertebrados del acuario, pero la mayoría ignora que el pH no se mide en una escala normal, sino en una escala logarítmica, lo que significa que un agua con un pH de 6 no es una séptima parte menos ácido que un agua con un pH de 7, sino diez veces más ácido. Y lo mismo pasa con un pH de 8 que no es una séptima parte más alcalino que un pH de 7, sino diez veces más.
En el hielo las moléculas no se mueven (vibran, pero se mantienen en posición), pero en el agua líquida las moléculas están en continuo movimiento, como ilustra el siguiente dibujo, donde en un recipiente largo con agua, en un extremo se añade unas gotas de tinta azul, y en el otro de tinta roja. Al comienzo una parte del agua del recipiente se colorea en rojo y la otra en azul, pero a medida que pasa el tiempo, las moléculas se mezclan y al final el color del agua, es morado (mezcla de azul y rojo). Esto ocurre porque las moléculas de agua tienen energía (más mientras más alta en la temperatura), que hace que se muevan continuamente.
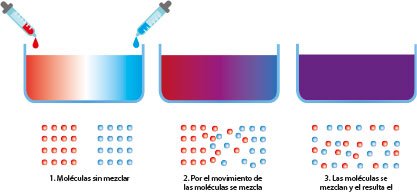
Cuando la temperatura del agua llega a los 100 grados centígrados (temperatura de ebullición), sus moléculas adquieren tanta energía que vencen la atracción entre sus partes negativas (cercanas al núcleo del átomo de Oxígeno) y sus partes positivas (cercanas a los núcleos de los átomos de Hidrógeno) y escapan al aire formando vapor de agua.
En la siguiente imagen vemos como se disponen las moléculas de agua en sus tres formas, hielo, agua líquida y vapor de agua (estado gaseoso).
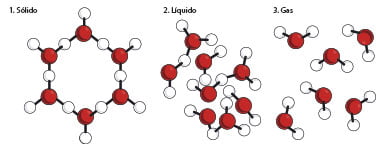
Cuando el agua está en estado líquido, la atracción entre los polos negativos y positivos de las mismas, las mantienen unidas, pero no estáticamente como ocurre cuando forman hielo, pues se mueven con más velocidad y energía a medida que aumenta la temperatura.
Conviene destacar, que las moléculas del agua se mueven y colisionan constantemente entre ellas, y que estas colisiones y la intensidad de las mismas aumentan con la temperatura, sencillamente porque la energía de las moléculas del agua se incrementa con la misma. A 25 grados de temperatura, en el agua destilada (nos referimos a agua pura), por cada 10 millones de moléculas de agua, un promedio de una molécula choca con otra con la energía y ángulo necesario, para romper las dos moléculas de agua, dando lugar a un ion hidronio (H3O+) y un ion de hidróxido (OH-), como se puede observar en la figura siguiente:
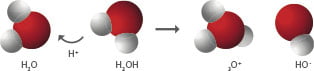
La diferencia entre los iones y las moléculas neutras como el agua, es que los iones tienen carga, en este caso negativa el ion Hidróxido OH- y positiva la del Hidronio H3O+, esto ocurre porque en las moléculas de agua, el número de electrones con carga negativa es el mismo, que el número de protones con carga positiva y por tanto no tienen carga o lo que es lo mismo son neutras, sin embargo cuando como consecuencia del choque se producen los iones el ion hidróxido OH-, mantiene un electrón más que protones, y por eso su carga es negativa. Es electrón es el que le falta al ion Hidronio H3O+, y en él que, por tanto, el número de protones con carga positiva es superior al de los electrones, lo que determina que su carga sea positiva.
Precisamente por tener carga los iones H3O+ (Hidronio) y OH- (Hidróxido), tienen una importancia extraordinaria en el agua de los acuarios, e incluso como explicaremos luego, en nuestra sangre, porque determinan el pH de la misma, que no es otra cosa que la medida de la acidez o alcalinidad del agua (o de la sangre), si el número de iones Hidronio (H3O+), es superior al del de iones Hidróxido (OH-), el agua tiene un pH ácido (inferior a 7) y si por el contrario es mayor el número de iones Hidróxido (OH-) que el de iones Hidronio (H3O+), el agua tiene un pH superior a 7 alcalino, y si el número de iones Hidronio (H3O+) es igual al de los iones Hidróxido (OH-), entonces el pH del agua es de 7, y es neutro.
Ejemplos de un ácido débil es el vinagre que tiene ácido acético, un ácido fuerte es el Clorhídrico conocido como agua fuerte o salfuman, y como compuestos alcalinos tenemos por ejemplo al bicarbonato sódico, que nos ayuda a contrarrestar la acidez del estómago, o la lejía.
En el caso del agua destilada, el pH es 7, lo que significa que existe un ion Hidronio (H3O+) y un ion hidróxido (OH-), por cada 10 millones de moléculas de agua, esto puede parecer una cifra pequeña, pero si recordamos que en una gota de agua hay algo más de mil seiscientos trillones de moléculas de agua, ello significa que existen en la misma gota unos 160 billones de iones Hidronio (para obtener esa cifra basta dividir la cantidad de 1.600 trillones de moléculas de agua en una gota, por 10 millones, que es la proporción de iones hidróxido e hidronio, que existen en una molécula de agua).
El porqué de que el pH del agua destilada es 7:
El pH se define como el logaritmo cambiado de signo, de la concentración en el agua de la concentración de iones Hidronio (H3O+), como la mayoría de ustedes se habrá olvidado de lo que es un logaritmo, les diremos que el pH define la mayor o menor acidez del agua (7 si es neutro, ácido si es menor de 7 y alcalino si es mayor). Sin embargo, una escala logarítmica no es como una escala normal, por ejemplo, un pH de 7.3, no es 3 décimas más alto que uno de 7, sino el doble, y un pH de 8 no es una unidad más alcalino que uno de 7, sino diez veces más. Por ello un cambio brusco del pH del agua, incluso de unas pocas décimas, puede matar a nuestros peces e invertebrados, porque al ser una escala logarítmica esa diferencia de décimas es mucho mayor que a una escala normal.
Con objeto de que conozcan mejor la química del acuario, vamos a explicarles lo que es un logaritmo, y por favor no se asusten porque es muy sencillo, lo vamos a ilustrar con un ejemplo:
10 elevado al cuadrado, se escribe 102 y es igual a 10 x 10 = 100. El logaritmo de 100 es 2, que no es otra cosa que el exponente o número de veces en que hay que multiplicar 10 por sí mismo para que de cien.
10 elevado al cubo, se escribe 103 y es igual a 10 x 10 x 10 = 1.000. El logaritmo de 1000 es 3, que no es otra cosa que el exponente o número de veces en que hay que multiplicar 10 por sí mismo, para que de mil.
10 elevado al sexto, se escribe 106 y es igual a 10 x 10 x 10 x 10 x 10 x 10 = 1.000.000. El logaritmo de 1.000.000 es 6, que no es otra cosa que el exponente o número de veces en que hay que multiplicar 10 para que de un millón.
En el caso del pH si este es neutro (pH=7), esto equivale a un ion Hidronio (H3O+) por cada diez millones de moléculas de agua, o lo que es lo mismo a 1 divido por 10 millones, que numéricamente es 1/10.000.000 (una diezmillonésima), que se escribe también como 1/107 (pues diez millones no es otra cosa que multiplicar a 10 por sí mismo siete veces), que se escribe también como 10-7, el exponente negativo significa que hay que dividir 1 por 10 elevado a 7, que nos da una diez millonésima, o lo que es lo mismo un ion Hidronio (H3O+) por cada diez millones de moléculas de agua.
Por tanto: 1/10.000.000 = 1/107 = 10-7, en este caso el logaritmo que corresponde a un ion de Hidronio por cada diez millones de moléculas de agua es el exponente a que hay que elevar el número diez, que en este caso es -7, como el pH es el logaritmo cambiado de signo, este es de – (-7) = 7.
Espero que esta explicación les haya ayudado a entender una escala logarítmica, pero si no ha sido así, recuerden que el pH lo que da es la mayor o menor concentración de iones hidronio, y que, al venir dado en una escala logarítmica, una pequeña diferencia de por ejemplo 3 décimas equivale al doble en una escala normal, por lo que un cambio brusco de pH del agua, de unas pocas décimas puede matar a nuestros peces e invertebrados.
Una de las formas de contribuir a la cura de peces de agua salada infectados por parásitos, es darle un baño de entre 5 y 10 minutos, en agua dulce, los peces toleran durante ese tiempo el cambio de salinidad, pero si no hemos igualado el pH del agua dulce mediante la adición de un poco de bicarbonato sódico, al del pH del acuario de agua salada del que provienen los peces a tratar, estos pueden morir por esa diferencia de pH. Pongo este ejemplo para realzar la importancia de no hacer cambios bruscos de pH, pues los peces aguantan unos minutos sin problema, un cambio muy grande de la salinidad, pero un brusco cambio en el pH de sólo unas décimas puede matarlos, porque como hemos explicado esas décimas vienen en una escala logarítmica, que es más del doble si el pH se midiera a una escala normal.
El porqué de que sea tan importante el pH:
El pH de nuestra sangre oscila entre 7,35 y 7,45, si el valor desciende de 7,1 o supera 7,8 nos puede producir la muerte, y algo parecido les pasa a los peces e invertebrados. Tanto ellos como nosotros tenemos unos mecanismos para contrarrestar un descenso o subida del pH, y en el caso de los peces un brusco cambio del pH del agua, implica que estos mecanismos de equilibrio pueden no tener tiempo suficiente para ajustar el pH de la sangre, lo que origina con frecuencia la muerte de los peces, de ahí que cuando enviamos peces (y cuando los recibimos de nuestros proveedores), recomendemos que se ajuste el pH de las bolsas al del acuario, antes de introducir a los peces en el mismo, lo cual se logra añadiendo pequeñas cantidades de agua (un vasito), cada tres o cuatro minutos, de agua del acuario a la bolsa, no bastando con doblar el volumen de la bolsa, cuando esto ocurre debe procederse a tirar la mitad, y volver a seguir añadiendo agua del acuario, hasta que la bolsa doble su volumen de nuevo.
Normalmente eso es suficiente, aunque lo ideal, es medir con un pH-metro el agua de las bolsas en que recibimos los peces o invertebrados y la del acuario, vamos añadiendo agua a la bolsa tal como hemos explicado, y sólo soltamos los peces en el acuario, cuando la diferencia entre los pH de la bolsa y del acuario, medidos con un pH-metro (se puede utilizar también un test de los que se venden en los comercios), es como mucho de dos décimas. Es recomendable recoger al pez en una red, y tirar el agua de la bolsa, introduciéndolo inmediatamente en el acuario.
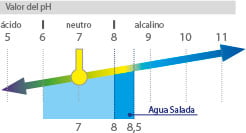
El pH en los acuarios marinos: Si medimos el pH del agua del mar, o el de un agua recién preparada con una buena sal marina, a 25 grados centígrados, el pH oscilará entre 8.1 y 8.3. Sin embargo, el pH del agua de un acuario marino tiende a acidificarse con el tiempo, ya que todos los organismos aerobios, que consumen oxígeno en el acuario, tales como bacterias nitrificantes, peces, corales y otros invertebrados, al consumir el oxígeno del agua emiten dióxido de carbono, también conocido como anhídrido carbónico, cuya fórmula es CO2. El anhídrido carbónico se combina con el agua para generar ácido carbónico de acuerdo con la siguiente reacción:
CO2 + H2O = CO3H2
El ácido carbónico va acidificando el agua del acuario disminuyendo su pH. El pH puede oscilar entre 7.5 y 8.5, pero aconsejamos que quede siempre en el intervalo de 7.7-8.3, teniendo en cuenta además que el pH de los acuarios desciende más por la noche, al no remover las algas el dióxido de carbono emitido por sus habitantes, pues para la fotosíntesis necesitan luz.
El pH y la reserva de alcalinidad (KH): Se denomina reserva de alcalinidad KH, el contenido de carbonatos y bicarbonatos del agua, mientras mayor es su cantidad, mayor es el pH. Se suele medir en grados, y deben oscilar entre 12 y 7 grados.
 Como mantener el pH en sus niveles adecuados: La mejor manera de mantener el pH en sus niveles óptimos, 8.1- 8.2, es mediante un cambio de un 10% de agua del acuario semanal, o de un 20% quincenal, de esa forma no sólo equilibramos el pH y el KH del agua, sino que añadimos elementos traza y rebajamos el contenido de fosfatos y nitratos de la misma.
Como mantener el pH en sus niveles adecuados: La mejor manera de mantener el pH en sus niveles óptimos, 8.1- 8.2, es mediante un cambio de un 10% de agua del acuario semanal, o de un 20% quincenal, de esa forma no sólo equilibramos el pH y el KH del agua, sino que añadimos elementos traza y rebajamos el contenido de fosfatos y nitratos de la misma.
También podemos alcanzar esos niveles mediante la adición se soluciones tampón que se venden en los comercios, que elevan el pH o el KH, en el último caso al elevar la reserva de alcalinidad KH, se eleva también el pH.
acuario, marino, ph, ph agua, qué es, todo sobre el ph, valores